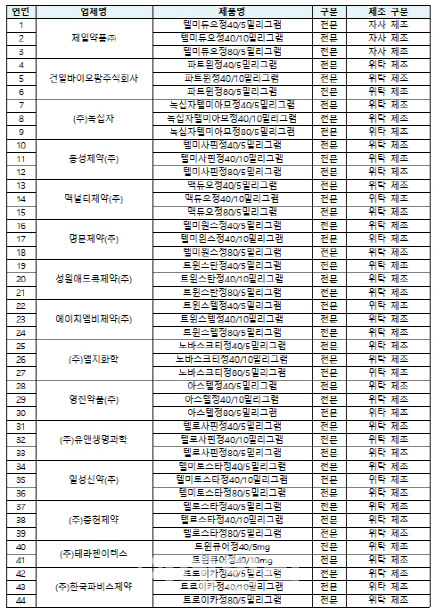
또 제일약품에서 ’텔미듀오정40/5밀리그램’ 등 3개 품목과 동일하게 위탁 제조하는 품목 중 동일한 허가 신청자료를 제출해 허가받은 14개사 41개 품목도 잠정 제조·판매 중지와 회수 조치하고 품목허가 취소 절차를 진행한다.
|
업체가 거짓·부정한 방법으로 품목허가를 받은 경우 약사법에 따라 해당 품목은 품목허가 취소 처분 절차가 진행된다.
식약처는 해당 44개 품목을 대체 의약품으로 전환하고 제품 회수가 적절히 수행되도록 의·약사 등 전문가의 협조를 요청하는 안전성 속보를 의·약사, 소비자 단체에 배포했다. 또 보건복지부와 건강보험심사평가원에 병·의원에서 해당 품목이 처방되지 않도록 조치해 줄 것을 요청했다.
식약처는 올해 4월부터 ‘의약품 GMP 특별 기획점검단’을 운영해 의약품 제조소에 대한 불시 점검을 연중 실시하고 있다.
|

.png)
.png)