|
캐나다 발리안트 파마슈티컬스(발리안스)가 개발한 말기 전립선암 환자 대상 ‘프로벤지’가 미국에서 시판된 유일한 암 치료 백신이다. 2010년 미국 식품의약국(FDA)의 승인을 획득한 프로벤지는 당시로선 생소했던 세포치료제 방식인데다 가격 대비 효능도 떨어져 흥행하진 못했다. 이후 많은 개발사가 pDNA나 펩타이드, mRNA, 면역세포의 일종인 수지상세포 등을 활용한 암 치료 백신 개발을 시도하는 상황이었다.
칸델, 바이러스 췌장암 백신...“2027년 허가가능성↑”
그런데 지난 12일(현지시간) 미국 식품의약국(FDA)이 칸델의 CAN-2409(아그라티마진 메사데노벡)을 췌장암 적응증에 한정해 패스트트랙으로 지정했다. 바이러스를 활용한 암백신 후보물질 중 최초로 패스트트랙으로 지정받았다.
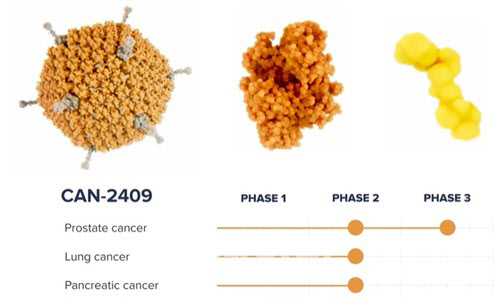
칸델은 CAN-2409는 전달체로 쓰인 아데노바이러스(AV)에 단순포진바이러스(HSV)에서 유래한 유전자를 삽입한 물질이다. 회사는 CARN2409와 함께 저분자성 경구약으로 항바이러스제(발라사이클로비르 등)를 투여하는 치료법으로 임상을 설계했다.
칸델에 따르면 CAN-2409 투여하면 단순포진바이러스의 유전자가 전달체를 통해 이동한 다음, 암세포를 선별적으로 감염시킨다. 이때 복용한 항바이러스제가 감염된 암세포를 골라 세포 사멸을 유도하는 기전이다. 회사 측은 이를 ‘바이러스 면역항암요법’이라고 명명하고 있다.
실제로 칸델은 CAN2409를 활용해 췌장암 및 비소세포폐암 대상 임상 2상을 진행 중이다. 또 회사는 해당 물질 관련 전립선암 대상 3상 연구를 추가로 진행 하고 있다. 이중 이번에 패스트트랙으로 지정된 췌장암 적응증에 대한 CAN2409의 임상 2a상의 중간 결과를 지난달 미국 ‘면역항암학회’(SITC)에서 발표하며 주목받았다. 여기에 따르면‘CAN2409’을 투약 후 3년 경과 시점에서 표준 췌장암 치료법(16.7%) 대비 약 4.3배 높은 71.4%의 생존률을 보인 것으로 확인되고 있다.
|
애스톤 “패스트트랙 밟지 않아...2028년 허가 목표”
한편 기존 암 치료 백신 개발사 중에선 애스톤사이언스와 머크·모더나 연합이 각각 pDNA와 mRNA 분야 물질로 최일선을 달리고 있다. 애스톤사이언스는 2028년, 머크 모더나 측은 2030년경 자체 개발중인 암 치료 백신을 미국에서 허가받는 것을 목표로 하고 있다.
애스톤사이언스는 pDNA 방식의 후보물질 3종(AST-301, AST-302, AST-201)과 펩타이드 방식 1종(AST-021p) 등 4종의 임상 단계 후보물질을 확보하고 있다. 이중 AST-301은 유방암 대상 미국 내 임상 2상을 진행 중이다. 회사 관계자는 “다양한 후보물질을 보유하고 있다 임상 단계가 다 다르다. 현재 진행 중인 임상 결과에 따라 각 물질별로 허가 시도 전략이 달라질 수 있다”이라고 설명했다.
또 코로나19를 통해 mRNA 백신이 세계적으로 각광받으면서 미국 모더나와 머크가 손을 잡고 해당 기술을 접목한 암 치료 백신 개발도 이뤄지고 있다. 실제로 양사는 지난 4월 mRNA 기반 암 치료 백신 후보물질 ‘mRNA-4157/V940’과 면역항암제 ‘키트루다’의 흑색종 환자 대상 병용요법에 대한 2b상에 성공한 바 있다.
mRNA나 DNA 방식의 암 치료 백신이 2030년 전후로 상용화 가도에 오를 전망이다. mRNA 코로나19 백신의 경우 팬데믹 상황에서 긴급 또는 조건부 승인되며 개발 1년 만에 도입됐지만, 기타 다른 질환에 대해선 미국에서 3상까지 모두 거쳐야 하는 상황이다. 모더나 측은 지난해 mRNA-4157/V940을 2030년경 출시하는 것을 목표로 한다고 밝힌 바 있다. 애스톤사이언스는 이보다 빠른 2028년경 AST-301을 미국에서 허가받는 것을 준비하고 있다고 내세우는 중이다.
한편 애스톤사이언스는 시리즈 A~C 투자를 통해 총 480억원의 투자금을 유치했으며, 지난달부터 코스닥 상장을 위한 기술성 평가를 밟기 위한 서류 작업이 한창인 것으로 확인됐다. 애스톤사이언스 관계자는 “기술성 평가 신청을 최근 완료하고 심사가 진행되고 있다. 그 결과를 기다리고 있으며 내년 상반기 상장하는 것이 목표다”고 전했다.
.png)