줄기세포치료제는 체내에서 오랫동안 남아 증식하면서 암세포로 변형되거나 타 세포들에 암성 변화를 촉진할 가능성이 높습니다. 또 치료제가 의도치 않은 신체부위로 이동해 원하지 않는 세포로 분화될 수도 있습니다.
CAR-T 치료제의 경우 ‘사이토카인 폭풍’과 신경독성 등 생명을 위협하는 부작용을 일으킬 수 있습니다. 사이토카인 폭풍은 외부에서 침입한 바이러스에 대항하기 위해 인체 내에서 면역작용이 과다하게 이뤄지면서 정상 세포까지 공격하는 현상을 말합니다.
최근엔 중간엽 줄기세포가 여타 줄기세포보다 안전성이 높은 것으로 판단돼 연구가 집중되고 있습니다. 또 유전자조작 줄기세포치료제 개발 시도도 활발하게 이뤄지고 있습니다. CAR-T는 사이토카인 폭풍에 대응해 항체나 스테로이드 등을 투여하는 방식으로 발전하고 있습니다.
T세포 대신 NK세포를 이용한 CAR-NK로 사이토카인 폭풍을 회피하는 연구도 부쩍 늘고 있습니다. 사이트카인 폭풍이나 신경 독성이 일어날 환자군을 미리 찾아내는 바이오마커 연구도 활발하게 진행 중입니다.
|
세포치료제의 또 다른 문제는 너무 비싼 데 있습니다. 노바티스 ‘킴리아’ 가격은 47만5000달러(5억5551만원)입니다. 입원료와 부작용 방지 처치료까지 합치면 100만달러(11억원)를 훌쩍 넘습니다. 보험처리가 되지 않는다면 일반 국민이 감당하기엔 너무 부담되는 액수입니다.
환자의 T세포를 채취해 냉동 보관한 뒤, 연구소로 보내 유전자조작을 통해 CAR-T로 만듭니다. 이를 다시 대량 배양시킨 뒤 동결시킵니다. 이 CAR-T는 병원에 보내져, 해동시킨 뒤 환자에게 주입합니다. 줄기세포치료제도 자가세포를 추출한 뒤 48시간 이내 다시 주입해야 합니다. 세포 배양해서 만들어낸 치료제를 본인 혼자만 쓸 수 있으므로 비쌀 수밖에 없습니다. 맞춤형 양복·구두가 기성복보다 비쌀 수밖에 없는 것과 같은 이치입니다. 특히 미국식품의약국(FDA)·EU·식약처의 GMP(의약품 제조·품질관리 기준)를 통과한 생산시설이 필요하고 전문 의약품 콜드체인을 통해서 생산된 세포치료제가 운반돼야 합니다. 또 숙련된 전문의 시술이 수반됩니다. 세포치료제 생산·운송 등 단계별로 고도화된 기술과 역량이 필요합니다.
세포치료제 이용이 보다 대중화되기 위해선 자기세포가 아닌 동종세포를 이용한 치료제 개발이 이뤄져야 합니다. 동종세포는 타인 세포를 환자가 이용할 수 있기 때문에 대량생산이 가능해 가격도 저렴합니다. 최근 크리스퍼(CRISPR-cas9) 유전자 가위의 유전자 편집 기술을 이용해 동종유래 세포의 면역반응을 해결하려는 연구가 활발하게 이뤄지고 있습니다. 동종세포 사용 제약이 사라진다면 세포치료제는 보다 대중화될 수 있습니다.
국내 바이오업체인 테고사이언스는 자기유래 세포치료제를 동종유래 세포치료제로 개발하려는 노력을 꾀하고 있습니다. 테고사이언스는 화상, 족부궤양 세포치료제는 이미 자기유래에서 동종유래 세포치료제 상용화에 성공했고, 동종유래 회전근개파열 치료제도 임상 2상을 진행 중입니다. 더디긴 하지만 자기유래와 더불어 동종유래 세포치료제로의 연구와 상업화에 성공한 치료제가 계속 등장하고 있습니다.
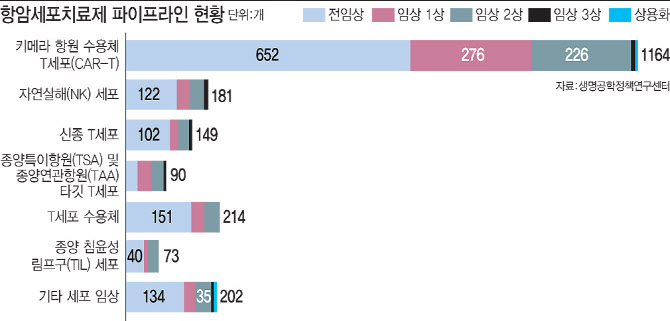
생명공학정책연구센터에 따르면 올해 4월 기준 전 세계 2073개의 항암세포치료제가 연구개발(R&D) 파이프라인에 있으며, 이 가운데 2/3는 자가유래이고 1/3은 동종유래 항암세포치료제로 연구중 입니다.

.png)
.png)