|
유럽 클리니컬트라이얼 1차지표도 실패
압타바이오 측은 지난 4일 ‘APX-115 당뇨병성 신증 임상 2상에 대한 압타바이오 입장 발표 전문’이라는 제목으로 공식 홈페이지에 입장문을 게시했다. 회사 측은 “클리니컬트라이얼은 미국 정부에서 운영하는 곳이다”며 “당사의 이번 임상은 유럽에서 진행된 것으로 유럽 정보공개 사이트에는 클리니컬트라이얼보다 훨씬 세부적인 내용이 공개돼 있다”고 밝혔다.
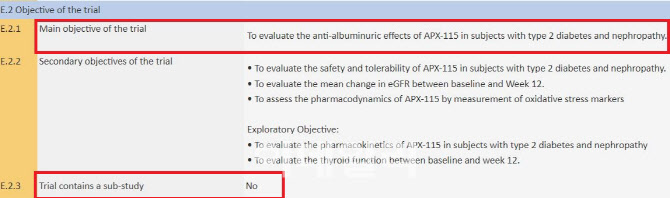
하지만 이데일리가 유럽 클리니컬트라이얼(EU Clinical Trials Register)에서 확인한 결과 1차지표는 미국 클리니컬트라이얼과 마찬가지로 단 한 개밖에 없는 것으로 드러났다. 12주 투약 후 전체 위약군 대비 전체 투약군의 UACR(소변 알부민 크리아티닌 비율) 변화 항목이다. 이밖에 2차지표는 3가지를 설정했다. 압타바이오는 공시에서 1차지표에 해당하는 결과는 통계 확보에 실패했다고 밝혔다. 11월 해외 학회 엠바고를 구실삼아 1차지표 P값을 공개하지 않았지만, 결국 P값이 0.05를 넘었다는 것을 의미한다. P값이 0.05를 넘을 경우 유의미한 약효가 없는 것으로 판단한다.
주목할 부분은 이번 임상 시험에서 서브 그룹에 대한 연구가 포함되지 않았다고 유럽 클리니컬트라이얼에 명시돼 있다는 점이다. 그럼에도 불구하고 압타바이오는 1차지표의 서브 그룹 분석 결과까지 모두 1차지표라고 볼 수 있다고 주장한다. 거래소가 지난달 29일 탑라인 공시에 1차지표의 서브 그룹까지 허용해준 이유 역시 압타바이오가 서브 그룹 분석 데이터 모두 1차지표라고 주장했기 때문인 것으로 전해진다.
만약 추후 공개 예정인 CSR(임상결과보고서)에서 1차지표와 2차지표가 아닌 서브 그룹 분석이었던 사실이 확인될 경우 거래소 제재는 불가피할 것으로 예상된다. 압타바이오는 ‘임상 2상 성공’이라는 제목으로 전 언론사에 보도자료를 배포했고, 2거래일 동안 주가가 50% 급등, 단기과열종목 지정예고까지 받았다. 지난해 금융감독원은 이와 비슷한 사례가 있었던 바이오회사에 대한 조사에 나선 바 있다. 당초 A사는 1차지표의 목표치에 도달하지 못했다고 밝혔다가, 3개월 만에 본인들에게 유리한 데이터를 바탕으로 임상에 성공했다고 말을 바꿨다.
|
◇1차지표 뒤에 적은 기저치 P값, 숨겨진 뜻은
지난달 29일 압타바이오 탑라인 공시에 따르면 “12주 투약 후, ITTS/FAS 분석군에서 UACR(소변 알부민 크리아티닌 비율)이 위약군에서는 약 3% 미만 감소한 것에 비해 APX-115 투약군에서는 약 20% 이상 감소했으나 통계적으로 유의하지 않았음”이라는 문장 바로 뒤에 “APX-115 투약군에서는 기저치 대비 UACR이 통계적으로 유의하게 감소함(P<0.05)”이라고 게시돼 있다.
일단 첫 번째 문장에서 통계적으로 유의하지 않았다고 밝힌 부분은 1차지표다. 두 번째 문장인 투약군의 기저치 대비 P값이 0.05 이하로 통계적 유의성을 확보했다고 한 것은 사실상 본인들에게 유리한 서브 그룹 데이터를 공시한 것으로 업계는 분석한다. 이는 투약군이 임상을 처음 시작할 때 대비 12주 약을 먹은 후의 개선된 수치를 비교한 것이다. 위약군과 투약군의 일대일 비교가 아닌 투약군에서만 데이터를 뽑아낸 결과다.
상장사 바이오회사 임상 담당 임원은 “환자들에게 투약하는 건데 그 약이 정말 물약이 아닌 이상에는 베이스라인 대비 당연히 효과는 나와야 한다. 약을 먹었기 때문에 나와야 하는 당연한 결과이며, 투약군의 기저치 분석을 1차지표라고 주장할 수 없다”며 “아마 CRO에서 투약군에 대해서만 기저치 분석을 해준 것처럼 위약군만으로 베이스라인 대비 얼마나 개선됐는지 명시했을 텐데 투약군만 공시한 것으로 보인다. 위약군에서도 기저치 대비 통계적으로 유의하게 얼마나 감소했는지 공개해야 한다”고 말했다.

.png)